Catalizadores y Enzimas
Por el Ing. Agr. Carlos González
![]()
Para armar una
molécula hacen falta muchos elementos, a saber:
1.
Materia prima con
la cual construir
2.
Operarios
especializados: las enzimas
3.
Transferencia de
electrones y de materiales preelaborados (dentro o fuera de la célula)
4.
Energía para unir
los átomos en las combinaciones deseadas.
Las enzimas son
las moléculas responsables de "elegir" entre una enorme cantidad de
reacciones posibles, cuáles de ellas van a ocurrir y cuáles no.
¿Cómo actúan las
enzimas?
Como vimos hasta
ahora, la velocidad de las reacciones dependen del
contacto entre las unidades químicas (átomos, moléculas, etc.), que a partir
del movimiento térmico (calor) producen colisiones entre esas mismas unidades.
Por lo tanto para cada temperatura existirá una velocidad de coalición
determinada.
La energía que se
necesita para que se produzca una reacción determinada se llama "energía
de activación".
Las reacciones
químicas que se dan siempre requieren de una gran energía de activación. Pero a
diferencia de lo que ocurre en un laboratorio, los organismos biológicos no
están preparados para soportar esa energía. Por ese motivo los sistemas vivos
han desarrollado un compuesto químico, que les sirve para llegar a una energía
de activación alta sin destruirse. Este compuesto se llama CATALIZADOR
, el cual aumenta la velocidad de coalición molecular sin calor
adicional produciendo un proceso llamado catálisis.
|
|
En la naturaleza existen diversos catalizadores, pero aquellos que son producidos por los organismos vivos se los conoce como catalizador biológico o ENZIMA.(*)
La enzima es un complemento para el
movimiento térmico, ósea disminuye los recursos de la energía activación
permitiendo una velocidad de reacción, a una temperatura inferior a la
realmente necesaria (fig.1).
¿Qué tipo de molécula es una enzima?
Las enzimas son proteínas de tipo globular, complejas.
¿Qué característica presenta?
a. Es específicas
a. Actúa en baja concentración
a. No sufre modificaciones
a. Se recupera intacta al final de la reacción
- No afecta el equilibrio de la reacción, pero sí su velocidad.(**)
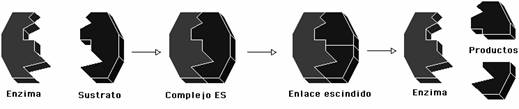
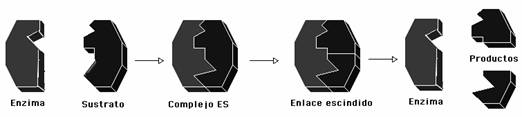
¿Cómo trabajan?
La enzima se une con una molécula
del sustrato para formar un complejo enzima-sustrato (ES), que, a su vez, se
disocia en el producto y la enzima, que se recupera:
![]()
El
sustrato es, casi siempre, más pequeño que la enzima y se une a ésta en un
lugar específico llamado sitio
activo. Típicamente, el sitio
activo es una pequeña abertura o hendidura en la estructura tridimensional de
la enzima.
Por lo
general, la concentración del sustrato es mayor que la de la enzima, [S] > [E],
por lo que los sitios activos se "llenan" rápidamente: la enzima se
satura. En este punto, el producto se forma a cierta velocidad (Vmax), no importa si se aumenta la [S].
Características
particulares del sitio activo:
(a)
Especificidad: una enzima puede discriminar entre diversas moléculas de
posibles sustratos. De aquí el axioma "una enzima para cada
sustrato". El sitio activo tiene una forma que se asemeja bastante al
sustrato, por lo que sustrato correcto se "ajusta perfectamente" en
el sitio activo.
(b)
Estructura: el sitio activo es una región tridimensional relativamente pequeña
de la enzima. Cuando está totalmente encajado, el sustrato interacciona
directamente con no más de
(c)
Interacciones: los sustratos son retenidos inicialmente en el sitio activo por
interacciones no covalente, débiles y reversibles, como
la interacciones hidrofóbicas, los puentes de
hidrógeno y los puentes salinos, que sostienen al sustrato orientado hacia los
residuos de aminoácidos para una mayor eficacia enzimática.
El
enlace escindido es el enlace que se va romper por la acción enzimática. Cuando el sustrato se une al sitio activo se
crea una tensión en ese enlace, que se rompe parcialmente en el estado de
transición. La energía necesaria surge de la energía liberada por la unión con
el sustrato. El estado de transición se estabiliza por la
interacciones no-covalentes que se forman.
Deprime la energía
de activación que se requiere en una reacción química, estableciendo una
asociación temporaria con la o las moléculas que reaccionan.
Cuando se establece la unión entre una
sustancia y una enzima se llama modelo "llave-cerradura". De
esta manera se establece la especificidad de la enzima y el producto. El ajuste
de esa unión se logra a través del sitio activo que presenta la
enzima.
Una vez lograda la reacción, la enzima se
separa del producto final quedando intacta para una futura intervención.
En la última década se ha observado que existe
otro tipo de enganche entre el sustrato y la enzima, y que consiste en que la
enzima tiene la particularidad de deformar y modificar su sitio activo el cual
se adapta a la del producto, este modelo se llama "ajuste inducido"
(fig.2).
|
|
Enzima + sustrato = enzima-sustrato (complejo
llave cerradura) = enzima + productos Enzima + sustratos = enzima sustratos (complejo ajuste inducido) = enzima +productos |
|
Formación de complejos enzima-sustrato (fig. 2) |
|
Muchas veces la actividad enzimática, puede modificarse de acuerdo a diversas razones
como por ejemplo necesidades metabólicas.
Uno de los ejemplos más
clásicos es la “inhibición por producto final”.
|
Enzima Q
Enzima H Enzima F Enzima U
INHIBICIÓN |
En
este caso se puede observar una serie de reacciones, cuyo producto final (Z),
es capaz de unirse a una enzima (Enzima Q) que cataliza a una sustancia A. El resultado final de esta acción es
la inhibición de dicha enzima, provocando que la cascada de reacciones no se
produzca y de esa manera no formar más el compuesto químico Z
(*)Generalmente, las enzimas se nombran
añadiendo la terminación "asa" a la raíz del nombre de la
sustancia sobre la actúan.
(**)La velocidad de las reacciones enzimáticas depende de la concentración del enzima, de la
concentración del sustrato (hasta un límite) y de la temperatura y el PH del
medio.
![]()